Винлеви®
WinleviТорговое наименование
Международное непатентованное наименование
Лекарственная форма
крем
Код АТХ
Листок-вкладыш: информация для пациентов
Винлеви® (класкотерон)
Крем 1%
Эти основные сведения не содержат всей информации, необходимой для безопасного и эффективного применения крема ВИНЛЕВИ. Полную информацию см. в полной инструкции по назначению крема ВИНЛЕВИ.
ВИНЛЕВИ® (класкотерон) крем для наружного применения
Первоначальное одобрение FDA: 2020
ПОКАЗАНИЯ И ПРИМЕНЕНИЕ
Крем ВИНЛЕВИ (класкотерон) является ингибитором рецепторов андрогенов и показан для наружного лечения вульгарных угрей у пациентов в возрасте 12 лет и старше.
РЕЖИМ ДОЗИРОВАНИЯ И СПОСОБ ПРИМЕНЕНИЯ
- Наносить тонкий слой (примерно 1 грамм) на поражённый участок два раза в день (утром и вечером). Избегать контакта с глазами, ртом и слизистыми оболочками.
- Не применять офтальмологически, перорально или вагинально.
ЛЕКАРСТВЕННАЯ ФОРМА И ДОЗИРОВКА
Крем 1%.
ПРОТИВОПОКАЗАНИЯ
Противопоказаний нет.
ПРЕДУПРЕЖДЕНИЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ
- Местное раздражение: При применении крема ВИНЛЕВИ могут развиться зуд, жжение, покраснение кожи или её шелушение. При появлении этих побочных эффектов следует прекратить применение или сократить частоту нанесения крема ВИНЛЕВИ.
- Подавление функции гипоталамо-гипофизарно-надпочечниковой (ГГН) оси: При проведении лечения класкотероном может развиться подавление функции ГГН оси.
- При развитии подавления функции ГГН оси следует предпринять попытку отменить препарат.
- Педиатрические пациенты могут быть более чувствительны к системной токсичности.
- Гиперкалиемия: Повышение уровня калия было отмечено у некоторых пациентов в ходе клинических испытаний.
НЕЖЕЛАТЕЛЬНЫЕ РЕАКЦИИ
Наиболее частые нежелательные реакции, встречающиеся в 7–12% случаев, включают эритему/покраснение, зуд и шелушение/сухость кожи. Кроме того, отёк, жжение встречались в более чем 3% случаев и отмечались примерно в такой же доле пациентов, получавших плацебо.
О подозреваемых нежелательных реакциях сообщайте в: Sun Pharmaceutical Industries, Inc. 1-800-818-4555 или в FDA по номеру 1-800-FDA-1088 или на веб-сайт www.fda.gov/medwatch.
Информацию для пациентов и рекомендованный FDA материал с информацией для пациентов см. в разделе 17.
СОДЕРЖАНИЕ ПОЛНОЙ ИНСТРУКЦИИ ПО НАЗНАЧЕНИЮ
1 ПОКАЗАНИЯ И ПРИМЕНЕНИЕ
2 РЕЖИМ ДОЗИРОВАНИЯ И СПОСОБ ПРИМЕНЕНИЯ
3 ЛЕКАРСТВЕННАЯ ФОРМА И ДОЗИРОВКА
4 ПРОТИВОПОКАЗАНИЯ
5 ПРЕДУПРЕЖДЕНИЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ
5.1. Местные кожные реакции
5.2. Подавление функции гипоталамо-гипофизарно-надпочечниковой (ГГН) оси
6 НЕЖЕЛАТЕЛЬНЫЕ РЕАКЦИИ
6.1. Опыт клинических испытаний
8 ПРИМЕНЕНИЕ В СПЕЦИАЛЬНЫХ КАТЕГОРИЯХ НАСЕЛЕНИЯ
8.1. Беременность
8.2. Лактация
8.3. Применение у детей
8.4. Применение у пожилых пациентов
11 ОПИСАНИЕ
12 КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ
12.1. Механизм действия
12.2. Фармакодинамика
12.3. Фармакокинетика
13 ДОКЛИНИЧЕСКАЯ ТОКСИКОЛОГИЯ
13.1. Канцерогенность, мутагенность, влияние на фертильность
14 КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
16КАК ПОЛУЧИТЬ/ХРАНЕНИЕ И ОБРАЩЕНИЕ
17 ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТОВ
Разделы или подразделы, отсутствующие в полной инструкции по назначению, не указаны.
Полная инструкция по назначению
1. ПОКАЗАНИЯ И ПРИМЕНЕНИЕ
Крем ВИНЛЕВИ (класкотерон) является ингибитором рецепторов андрогенов и показан для наружного лечения вульгарных угрей у пациентов в возрасте 12 лет и старше.
2. РЕЖИМ ДОЗИРОВАНИЯ И СПОСОБ ПРИМЕНЕНИЯ
Аккуратно очистить поражённый участок кожи. После того как кожа высохнет, нанести тонкий равномерный слой крема ВИНЛЕВИ два раза в день, утром и вечером, на поражённый участок. Избегать случайного попадания крема ВИНЛЕВИ в глаза, рот или другие слизистые оболочки. При контакте со слизистыми оболочками тщательно промыть водой.
Крем ВИНЛЕВИ предназначен только для наружного применения. Крем ВИНЛЕВИ не предназначен для офтальмологического, перорального или вагинального применения.
3. ЛЕКАРСТВЕННАЯ ФОРМА И ДОЗИРОВКА
Крем 1%. Каждый грамм крема ВИНЛЕВИ содержит 10 мг класкотерона в белом или почти белом креме.
4. ПРОТИВОПОКАЗАНИЯ
Противопоказаний нет.
5. ПРЕДУПРЕЖДЕНИЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ
5.1 Местные кожные реакции
Крем ВИНЛЕВИ может вызывать местное раздражение (эритему/покраснение, зуд, шелушение/сухость). Одновременное применение с другими потенциально раздражающими наружными препаратами (лекарственные или абразивные мыла и очищающие средства, мыла и косметические средства с сильным высушивающим эффектом, а также продукты с высокой концентрацией спирта, вяжущих веществ, пряностей или лайма) следует ограничивать.
Препарат не должен наноситься на порезы, ссадины, области с экземой или солнечными ожогами.
5.2 Подавление функции гипоталамо-гипофизарно-надпочечниковой (ГГН) оси
При проведении лечения класкотероном было зафиксировано и может развиться подавление функции ГГН оси. В исследовании фармакокинетики все пациенты восстановили нормальную функцию ГГН оси при контрольном осмотре через 4 недели после завершения лечения (см. раздел 12.2 о клинической фармакологии). Условия, усиливающие системное всасывание, включают применение на больших поверхностях кожи, длительное применение и использование окклюзивных повязок.
При развитии подавления функции ГГН оси следует предпринять попытку отменить препарат.
Педиатрические пациенты могут быть более чувствительны к системной токсичности.
6. НЕЖЕЛАТЕЛЬНЫЕ РЕАКЦИИ
6.1 Опыт клинических испытаний
Поскольку клинические испытания проводятся в самых различных условиях, частота нежелательных реакций, наблюдаемая при клинических испытаниях одного препарата, не может быть напрямую сравнима с частотой при клинических испытаниях другого препарата и может не отражать частоту, наблюдаемую на практике.
В двух идентичных многоцентровых рандомизированных двойных слепых плацебо-контролируемых исследованиях 1421 пациент в возрасте 12 лет и старше с вульгарными угрями лица применял крем ВИНЛЕВИ или плацебо два раза в день в течение 12 недель. В целом 62% пациентов были женщины, 38% были мужчины, 91% пациентов были кавказцами, средний возраст составил 19,7 года.
Местные кожные реакции (отёк, эритема/покраснение, зуд, шелушение/сухость, атрофия кожи, жжение/пощипывание, рубеолярные полосы, телеангиэктазия) наблюдались в течение 12-недельного периода лечения и встречались в такой же доле пациентов, получавших плацебо. Местные кожные реакции, о которых сообщалось у ≥1% пациентов, получавших крем ВИНЛЕВИ, представлены в следующей таблице.
| Таблица 1. Частота новых или ухудшившихся местных кожных реакций, о которых сообщалось у ≥1% пациентов, получавших крем ВИНЛЕВИ, после 1-го дня в 12-недельных контролируемых клинических исследованиях | ||
|---|---|---|
| Крем ВИНЛЕВИ 1% (N=674*) | Крем плацебо (N=656*) | |
| Отёк | 24 (3,6%) | 23 (3,5%) |
| Эритема/покраснение | 82 (12,2%) | 101 (15,4%) |
| Зуд | 52 (7,7%) | 54 (8,2%) |
| Шелушение/сухость | 71 (10,5%) | 68 (10,4%) |
| Атрофия кожи | 11 (1,6%) | 17 (2,6%) |
| Жжение/пощипывание | 28 (4,2%) | 28 (4,3%) |
| Рубеолярные полосы | 17 (2,5%) | 10 (1,5%) |
| Телеангиэктазия | 8 (1,2%) | 12 (1,8%) |
*Знаменатели для расчёта процентов составляли 674 из 709 пациентов, получавших крем ВИНЛЕВИ, и 656 из 712 пациентов, получавших плацебо в этих исследованиях, у которых были получены результаты местных кожных реакций после 1-го дня.
Следующие нежелательные реакции, связанные с применением крема ВИНЛЕВИ, были выявлены в клинических исследованиях и долгосрочных исследованиях безопасности.
Обмен веществ: гиперкалиемия (см. раздел 12.2 о клинической фармакологии)
Репродуктивная система: поликистоз яичников, аменорея.
8. ПРИМЕНЕНИЕ В СПЕЦИАЛЬНЫХ КАТЕГОРИЯХ НАСЕЛЕНИЯ
8.1 Беременность
Краткое резюме риска
Не имеется доступных данных о применении крема ВИНЛЕВИ у беременных женщин, которые позволили бы оценить вызванный препаратом риск серьёзных врождённых дефектов, выкидыша или неблагоприятных исходов беременности или плода. В исследованиях репродуктивной токсичности на животных при подкожном введении класкотерона беременным крысам и кроликам в период органогенеза при дозах в 8 и 39 раз выше максимально рекомендуемой дозы для человека (МРДЧ) соответственно наблюдалось увеличение количества пороков развития у крыс и постимплантационных потерь и резорбции у кроликов (см. раздел «Данные»).
Фоновый риск серьёзных врождённых дефектов и выкидыша для обозначенной категории пациентов неизвестен. Неблагоприятные исходы при беременности происходят независимо от состояния здоровья матери или применения лекарственных препаратов. В общей популяции США предполагаемый фоновый риск серьёзных врождённых дефектов и выкидыша при клинически признанных беременностях составляет 2–4% и 15–20% соответственно.
Данные
Данные на животных
В исследовании внутриутробного развития класкотерон вводился подкожно беременным крысам в дозах 1, 5 или 25 мг/кг/день в период органогенеза. При дозах вплоть до 25 мг/кг/день (336 раз превышающих МРДЧ на основе сравнения площади под кривой концентрация-время) не отмечалось связанной с класкотероном материнской токсичности или воздействия на параметры матки. Пороки развития, связанные с класкотероном, были отмечены при всех уровнях доз без установления зависимости от дозы. Омфалоцеле было отмечено у одного плода при каждом уровне дозы. Внешние и висцеральные пороки развития (выраженное расширение боковых и третьего желудочков головного мозга, тонкая кожа, уменьшение размеров и высовывающийся язык) были отмечены ещё у двух плодов при дозе 1 мг/кг/день (8 раз превышающей МРДЧ на основе сравнения площади под кривой концентрация-время).
В исследовании внутриутробного развития класкотерон вводился подкожно беременным кроликам в дозах 0,1, 0,4 или 1,5 мг/кг/день в период органогенеза. Постимплантационные потери и резорбции были увеличены при дозе 1,5 мг/кг/день (39 раз превышающей МРДЧ на основе сравнения площади под кривой концентрация-время). При дозах вплоть до 0,4 мг/кг/день (12 раз превышающих МРДЧ на основе сравнения площади под кривой концентрация-время) развитая токсичность не отмечалась. Связанная с классотероном материнская токсичность или пороки развития плода не были отмечены при дозах вплоть до 1,5 мг/кг/день (39 раз превышающих МРДЧ на основе сравнения площади под кривой концентрация-время).
В исследовании пренатального и постнатального развития класкотерон вводился подкожно беременным крысам в дозах 0,5, 2,5 и 12,5 мг/кг/день, начиная с дня беременности 6 и продолжая на протяжении дня лактации 20. Значительная материнская или развитая токсичность не наблюдалась при дозах вплоть до 12,5 мг/кг/день (163 раза превышающих МРДЧ на основе сравнения площади под кривой концентрация-время).
8.2 Лактация
Краткое резюме риска
Отсутствуют данные о наличии класкотерона или его метаболитов в грудном молоке, влиянии на грудного ребёнка или воздействии на лактацию. Отсутствие клинических данных при лактации исключает возможность ясного определения риска класкотерона для младенца в период лактации; поэтому следует учитывать как пользу для развития и здоровья грудного вскармливания, так и клиническую необходимость применения класкотерона матерью и любое потенциальное неблагоприятное воздействие на вскармливаемого ребёнка класкотерона или основного материнского заболевания.
8.4 Применение у детей
Безопасность и эффективность крема ВИНЛЕВИ для наружного лечения вульгарных угрей были установлены у 641 педиатрического пациента в возрасте 12–18 лет в двух идентичных многоцентровых рандомизированных двойных слепых плацебо-контролируемых 12-недельных исследованиях и 2 открытых исследованиях фармакокинетики (см. раздел 14 о клинических исследованиях).
Безопасность и эффективность крема ВИНЛЕВИ для наружного лечения вульгарных угрей не были установлены у педиатрических пациентов моложе 12 лет.
Подавление функции гипоталамо-гипофизарно-надпочечниковой (ГГН) оси было зафиксировано у 2 из 22 (9%) подростков. Все пациенты восстановили нормальную функцию ГГН оси при контрольном осмотре через 4 недели после завершения лечения (см. раздел 12.2 о клинической фармакологии). Дети могут быть более чувствительны к системной токсичности при лечении класкотероном (см. раздел 12.2 о фармакодинамике).
8.5 Применение у пожилых пациентов
В клинических исследованиях крема ВИНЛЕВИ не участвовало достаточного количества пациентов в возрасте 65 лет и старше, чтобы определить, отличается ли их ответ на препарат от ответа у более молодых пациентов. Другой имеющийся клинический опыт не выявил различий в ответах между пожилыми и более молодыми пациентами. Вообще, выбор дозы для пожилого пациента должен быть осторожным, обычно начиная с низкого конца диапазона дозирования, отражая большую частоту сниженной функции печени, почек или сердца, сопутствующих заболеваний или других лекарственных взаимодействий.
11. ОПИСАНИЕ
Крем ВИНЛЕВИ (класкотерон) содержит класкотерон, ингибитор рецепторов андрогенов, в основе крема для наружного дерматологического применения. Крем ВИНЛЕВИ представляет собой белый или почти белый крем.
По химической структуре класкотерон — это кортексолон-17α пропионат. Класкотерон представляет собой белый или почти белый порошок, практически нерастворимый в воде. Соединение имеет эмпирическую формулу C₂₄H₃₄O₅ и молекулярную массу 402,5 г/моль. Структурная формула представлена ниже.
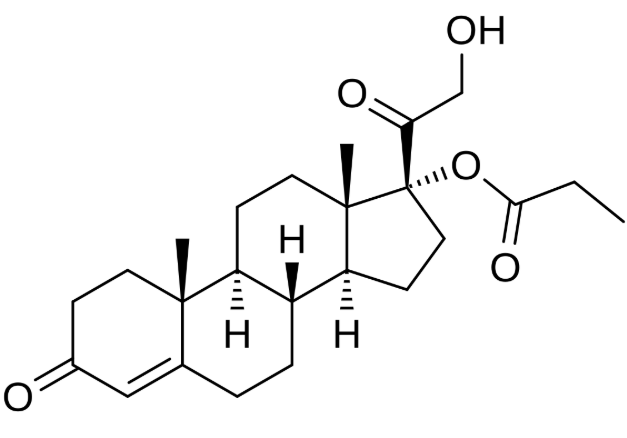
Каждый грамм крема ВИНЛЕВИ 1% содержит 10 мг класкотерона в основе крема, состоящей из цетилового спирта, лимонной кислоты моногидрата, динатриевой соли этилендиаминтетрауксусной кислоты, минерального масла, моно- и диглицеридов, полисорбата 80, пропиленгликоля, очищенной воды и витамина E.
12. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ
12.1 Механизм действия
Класкотерон является ингибитором рецепторов андрогенов. Механизм действия крема ВИНЛЕВИ для наружного лечения вульгарных угрей неизвестен.
12.2 Фармакодинамика
Подавление функции гипоталамо-гипофизарно-надпочечниковой (ГГН) оси
Подавление функции ГГН оси было оценено у взрослых (n=20) и подростков (n=22) с вульгарными угрями после двукратного ежедневного применения крема ВИНЛЕВИ в течение 2 недель в исследовании фармакокинетики, описанном в разделе 12.3. Подавление функции ГГН оси, указываемое уровнем кортизола в сыворотке крови через 30 минут после стимуляции ≤18 мкг/дл, было зафиксировано у 1 из 20 (5%) взрослых пациентов и у 2 из 22 (9%) подростков на 14-й день. Все пациенты восстановили нормальную функцию ГГН оси при контрольном осмотре через 4 недели после завершения лечения.
Калий
Смещение от нормальных значений к повышенным уровням калия было зафиксировано у 5% пациентов, получавших класкотерон, и у 4% пациентов, получавших плацебо.
Электрофизиология сердца
При примерно 2-кратном системном воздействии, наблюдаемом при максимальной дозе, крем ВИНЛЕВИ не удлиняет интервал QT в какой-либо клинически значимой степени.
12.3 Фармакокинетика
Абсорбция
После наружного применения крема ВИНЛЕВИ в течение 2 недель со средней дозой примерно 6 граммов, применяемой два раза в день, у взрослых пациентов с умеренно-тяжелыми вульгарными угрями (n=20), системные концентрации класкотерона достигли равновесного состояния к 5-му дню. На 14-й день среднее ± стандартное отклонение максимальной концентрации в плазме крови (Сmax) составило 4,5 ± 2,9 нг/мл, среднее ± стандартное отклонение площади под кривой концентрация-время в течение интервала дозирования (AUC) составило 37,1 ± 22,3 ч·нг/мл, и среднее ± стандартное отклонение средней концентрации в плазме крови (Cavg) составило 3,1 ± 1,9 нг/мл.
Распределение
Связывание класкотерона с белками плазмы крови составляет 84–89% и не зависит от концентраций в условиях in vitro.
Элиминация
Метаболизм
После наружного применения крема ВИНЛЕВИ концентрации кортексолона, возможного первичного метаболита класкотерона, были определены и в целом находились ниже или вблизи нижнего предела определения (0,5 нг/мл) у пациентов ≥12 лет с вульгарными угрями.
Исследование in vitro показало, что инкубация 10 мкмоль/л класкотерона с криоконсервированными гепатоцитами человека привела к образованию кортексолона в качестве возможного первичного метаболита и других неидентифицированных метаболитов, включая конъюгированные метаболиты.
Выведение
Выведение класкотерона полностью не охарактеризовано в организме человека.
Специальные категории пациентов
Педиатрические пациенты
У подростков ≥12 и <18 лет (n=22) после 2 недель двукратного ежедневного применения со средней дозой примерно 6 граммов крема ВИНЛЕВИ (или со средней дозой примерно 4 граммов у более молодых, менее крупных пациентов) концентрации класкотерона в равновесном состоянии были достигнуты к 5-му дню. Системное воздействие класкотерона у подростков было аналогично наблюдаемому у взрослых.
Исследования взаимодействия лекарственных препаратов
Клинические исследования
Никакие клинические исследования, оценивающие потенциал взаимодействия лекарственных препаратов при применении крема ВИНЛЕВИ, не проводились.
Исследования in vitro
Ферменты цитохрома P450: Класкотерон ингибировал CYP 1A2, 2B6, 2C8, 2C9, 2C19, 2D6, 2E1 или 3A4 со значением IC50 >40 мкмоль/л. Класкотерон вплоть до 30 мкмоль/л не индуцировал CYP 1A2, 2B6 или 3A4. Эти результаты предполагают, что крем ВИНЛЕВИ не оказывает клинически значимого влияния на фармакокинетику препаратов, метаболизируемых CYP 1A2, 2B6, 2C8, 2C9, 2C19, 2D6, 2E1 или 3A4.
13. ДОКЛИНИЧЕСКАЯ ТОКСИКОЛОГИЯ
13.1 Канцерогенность, мутагенность, влияние на фертильность
Крем класкотерона (0,1%, 1% или 5%) не проявлял канцерогенный эффект после ежедневного наружного применения в 2-летнем исследовании канцерогенности на крысах. О повышенной частоте неопластического поражения в виде атрофии кожи и подкожной клетчатки в месте применения было сообщено у самцов и самок, получавших крем класкотерона 1% и 5%.
Класкотерон не был мутагенным в тесте обратной мутации Эймса и не был кластогенным в исследовании хромосомных аберраций лимфоцитов человека in vitro. При введении крысам через подкожную инъекцию класкотерон не индуцировал микроядра в костном мозге при дозах 500 или 1000 мг/кг, но незначительное увеличение микроядер произошло у 2 из 5 крыс при дозе 2000 мг/кг. Реакция была расценена как неоднозначная. В целом, совокупность доказательств указывает на то, что класкотерон не представляет генотоксический риск.
В исследовании фертильности и раннего развития эмбриона у крыс класкотерон вводился подкожно в дозах 0,5, 2,5 или 12,5 мг/кг/день с 2–4 недель до спаривания и во время спаривания. Класкотерон увеличил преимплантационные потери при дозе 12,5 мг/кг/день (163 раза превышающей МРДЧ на основе сравнения площади под кривой концентрация-время). Класкотерон не оказал влияния на спаривание или фертильность у крыс при дозах вплоть до 12,5 мг/кг/день (163 раза превышающих МРДЧ на основе сравнения площади под кривой концентрация-время). Никаких влияний на развитие не было отмечено при дозах вплоть до 2,5 мг/кг/день (33 раза превышающих МРДЧ на основе сравнения площади под кривой концентрация-время).
14. КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Безопасность и эффективность крема ВИНЛЕВИ 1% при применении два раза в день в течение 12 недель для лечения вульгарных угрей были оценены в двух одинаково спланированных многоцентровых рандомизированных двойных слепых плацебо-контролируемых клинических исследованиях (Исследование 1 [NCT02608450] и Исследование 2 [NCT02608476]), в которых участвовало 1440 пациентов с вульгарными угрями лица. В исследованиях участвовали пациенты в возрасте 9 лет и старше с оценкой по шкале Investigator's Global Assessment (IGA) умеренных или тяжёлых вульгарных угрей лица (оценка 3 или 4), 30–75 воспалительных элементов (папулы, пустулы и узелки) и 30–100 невоспалительных элементов (открытые и закрытые комедоны).
Всего в исследование было включено 1421 пациентов в возрасте 12 лет и старше с вульгарными угрями лица. Из этих пациентов 641 (45%) были в возрасте 12–17 лет, а 780 (55%) были в возрасте 18 лет и старше. Кроме того, 62% пациентов были женщины, 91% были кавказцы. В начале исследования пациенты имели среднее количество воспалительных элементов 42,4 и среднее количество невоспалительных элементов 61,4. Кроме того, примерно 83% пациентов имели оценку по шкале IGA 3 («умеренные угри»).
Эффективность была оценена на 12-й неделе по доле пациентов в каждой группе лечения, у которых отмечалось снижение показателя IGA как минимум на 2 балла по сравнению с исходным значением, и по оценке IGA 0 (чистая кожа) или 1 (почти чистая кожа), абсолютное изменение и процентное изменение с исходного значения количества невоспалительных и воспалительных элементов. Частота ответа по шкале IGA и среднее абсолютное и процентное снижение с исходного значения количества элементов угревой сыпи через 12 недель лечения у пациентов в возрасте 12 лет и старше представлены в следующей таблице.
| Таблица 2. Клиническая эффективность крема ВИНЛЕВИ 1% у пациентов с вульгарными угрями на 12-й неделе | ||||
|---|---|---|---|---|
| Исследование 1 | Исследование 2 | |||
| Крем ВИНЛЕВИ 1% N=342 | Крем плацебо N=350 | Крем ВИНЛЕВИ 1% N=367 | Крем плацебо N=362 | |
| Успех по шкале IGA* | 18,8% | 8,7% | 20,9% | 6,6% |
| Разница с плацебо (95% ДИ) | 10,1% (4,1%, 16,0%) | 14,3% (8,9%, 19,7%) | ||
| Невоспалительные элементы | ||||
| Среднее абсолютное снижение | 20,4 | 13,0 | 19,5 | 10,8 |
| Разница с плацебо (95% ДИ) | 7,3 (3,5, 11,1) | 8,7 (4,5, 12,4) | ||
| Среднее процентное снижение | 32,6% | 21,8% | 29,6% | 15,7% |
| Разница с плацебо (95% ДИ) | 10,8% (3,9%, 17,6%) | 13,8% (7,5%, 20,1%) | ||
| Воспалительные элементы | ||||
| Среднее абсолютное снижение | 19,3 | 15,4 | 20,1 | 12,6 |
| Разница с плацебо (95% ДИ) | 3,9 (1,3, 6,5) | 7,5 (5,2, 9,9) | ||
| Среднее процентное снижение | 44,6% | 36,3% | 47,1% | 29,7% |
| Разница с плацебо (95% ДИ) | 8,3% (2,2%, 14,4%) | 17,5% (11,8%, 23,1%) | ||
* Успех по шкале IGA определялся как снижение показателя IGA как минимум на 2 балла по сравнению с исходным значением и оценка по шкале IGA 0 (чистая кожа) или 1 (почти чистая кожа).
16. КАК ПОЛУЧИТЬ/ХРАНЕНИЕ И ОБРАЩЕНИЕ
Крем ВИНЛЕВИ 1% поставляется в алюминиевой тубе с закрытым дном с эпоксидным покрытием и колпачком из полипропилена:
NDC 47335-994-36
Туба 60 граммов
До отпуска: Хранить продукт в холодильнике при температуре от 2°C до 8°C (от 36°F до 46°F). Не замораживать.
Инструкции по хранению для фармацевта: Направить пациента хранить продукт при использовании при комнатной температуре от 20°C до 25°C (от 68°F до 77°F). Не замораживать. Неиспользованный продукт должен быть утилизирован через 180 дней с момента отпуска или через 1 месяц после первого открытия, в зависимости от того, что произойдёт раньше.
17. ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТОВ
- Рекомендуйте пациенту ознакомиться с рекомендованной FDA информацией для пациентов.
- Избегайте применения крема ВИНЛЕВИ на повреждённой коже (таких как порезы, ссадины), участках с экземой и на солнечных ожогах.
- Избегайте одновременного применения других потенциально раздражающих наружных продуктов (медикаментозных или иных).
Информация для пациентов
ВИНЛЕВИ (Вин-ле-ви)
(класкотерон) крем
Важная информация:
Крем ВИНЛЕВИ предназначен только для применения на коже (наружное применение). Не используйте крем ВИНЛЕВИ в глазах, ротовой полости или влагалище и на них.
Что такое крем ВИНЛЕВИ?
Крем ВИНЛЕВИ — это рецептурный препарат, применяемый на коже (наружное применение) для лечения вульгарных угрей у людей в возрасте 12 лет и старше.
Неизвестно, является ли крем ВИНЛЕВИ безопасным и эффективным у детей моложе 12 лет.
Перед применением крема ВИНЛЕВИ
Перед использованием крема ВИНЛЕВИ сообщите своему врачу обо всех своих медицинских состояниях, включая следующие:
- проблемы с кожей, включая экзему, порезы или солнечные ожоги
- беременность или планирование беременности. Неизвестно, будет ли крем ВИНЛЕВИ вредить вашему будущему ребёнку.
- кормление грудью или планирование кормления грудью. Неизвестно, попадает ли крем ВИНЛЕВИ в грудное молоко. Поговорите со своим врачом о лучшем способе кормления ребёнка во время лечения кремом ВИНЛЕВИ.
Сообщите своему врачу о лекарствах, которые вы принимаете, включая рецептурные и безрецептурные лекарства, витамины и растительные добавки.
Как применять крем ВИНЛЕВИ?
- Применяйте крем ВИНЛЕВИ точно так, как вам говорит ваш врач.
- Перед применением крема ВИНЛЕВИ аккуратно вымойте и высушите поражённый участок кожи.
- После высыхания кожи нанесите тонкий равномерный слой крема ВИНЛЕВИ на поражённые участки 2 раза в день, утром и вечером.
- Вымойте руки после применения крема ВИНЛЕВИ.
Что следует избегать при применении крема ВИНЛЕВИ?
- Избегайте использования крема ВИНЛЕВИ на участках кожи с порезами, ссадинами, экземой или на солнечных ожогах.
- Избегайте попадания крема ВИНЛЕВИ в глаза, губы, рот, углы носа или на слизистые оболочки. При попадании на слизистые оболочки тщательно промойте водой.
Избегайте применения средств для ухода за кожей, которые могут высушивать или раздражать вашу кожу, таких как:
◦ лекарственные или абразивные мыла и очищающие средства
◦ мыла, очищающие средства и косметические средства с сильным высушивающим эффектом
◦ продукты с высокой концентрацией спирта
- вяжущие вещества, пряности или лайм
Какие возможны побочные эффекты крема ВИНЛЕВИ?
Крем ВИНЛЕВИ может вызывать серьёзные побочные эффекты, включая:
- Местные кожные реакции. Крем ВИНЛЕВИ может вызывать местное раздражение кожи, включая зуд, жжение, покраснение кожи или её шелушение.
- Симптомы состояния, при котором надпочечник не вырабатывает достаточное количество определённых гормонов (надпочечниковая недостаточность) во время лечения кремом ВИНЛЕВИ. Ваш врач может остановить ваше лечение кремом ВИНЛЕВИ, если у вас разовьются какие-либо проблемы с надпочечниками.
Наиболее частые побочные эффекты крема ВИНЛЕВИ включают покраснение, шелушение или сухость и зуд обрабатываемой кожи.
Это не полный список возможных побочных эффектов крема ВИНЛЕВИ.
Проконсультируйтесь со своим врачом о побочных эффектах. Вы можете сообщить о побочных эффектах в FDA по номеру 1-800-FDA-1088. Вы также можете сообщить о побочных эффектах компании Sun Pharmaceutical Industries, Inc., позвонив по номеру 1-800-818-4555.
Как хранить крем ВИНЛЕВИ?
- Хранить крем ВИНЛЕВИ при комнатной температуре от 20°C до 25°C (от 68°F до 77°F). Не замораживать.
- Утилизировать (выбросить) неиспользованную часть через 180 дней с момента отпуска или через 1 месяц после первого открытия, в зависимости от того, что произойдёт раньше.
- Храните крем ВИНЛЕВИ и все лекарства в недоступном для детей месте.
Общая информация о безопасном и эффективном применении крема ВИНЛЕВИ
Лекарства иногда назначаются в целях, которые не указаны в листке-вкладыше для пациентов. Не применяйте крем ВИНЛЕВИ при состоянии, при котором он вам не был назначен. Не давайте крем ВИНЛЕВИ другим людям, даже если у них те же симптомы, что и у вас. Это может им навредить. Вы можете попросить информацию о креме ВИНЛЕВИ у своего врача или фармацевта, которая предназначена для медицинских работников.
Какие ингредиенты содержит крем ВИНЛЕВИ?
Действующее вещество: класкотерон
Вспомогательные вещества: цетиловый спирт, лимонная кислота моногидрат, динатриевая соль этилендиаминтетрауксусной кислоты, минеральное масло, моно- и диглицериды, полисорбат 80, пропиленгликоль, очищенная вода и витамин E.
Произведено в Италии для: Sun Pharmaceutical Industries Limited
Распределение: Sun Pharmaceutical Industries, Inc., Cranbury, NJ 08512
ВИНЛЕВИ — лицензионная торговая марка компании Cassiopea, S.p.A., исключительно лицензированная компанией Sun Pharmaceutical Industries Limited
Патенты США: https://www.cassiopea.com/patents
© 2021 Sun Pharmaceutical Industries Limited. Все права защищены.
Одобрено Управлением по контролю качества пищевых продуктов и лекарственных средств США (FDA)
▼ Лекарственный препарат в настоящий момент не зарегистрирован в Российской Федерации. |
Форма выпуска
Крем 1 %.
Условия отпуска из аптек
Отпускают по рецепту
